UNSUR
BAHAN AJAR
HARI / TANGGAL : Rabu / 16 - 10 - 2019
KELAS : 7B, 7C, 7A
SEMESTER : Ganjil
Jam
Pertemuan
|
Kompetensi Dasar/ Indikator Pencapaian Kompetensi
|
Tujuan Pembelajaran
|
Langkah-langkah Pembelajaran
|
Sumber Belajar/Alat Peraga
|
Instrumen Penilaian
|
Ket
|
KD. 3.3
Memahami
konsep campuran dan zat tunggal (unsur dan senyawa), sifat fisika dan
kimia, perubahan fisika dan kimia dalam kehidupan sehari-hari
IPK.
3.3.1 Menggolongkan karakteristik materi.
3.3.2 Menjelaskan perbedaan unsur, senyawa, dan campuran.
3.3.3 Menjelaskan metode pemisahan campuran.
|
§ Dengan diberikan daftar benda yang digunakan dalam kehidupan sehari-hari Peserta Didik dapat menggolongkan karakteristik materi.
§ Dengan diberikan LKS Peserta Didik dapat menjelaskan perbedaan unsur, senyawa, dan campuran.
§ Dengan melakukan percobaan, Peserta Didik dapat menyelidiki bahan-bahan alam yang dapat dijadikan sebagai Indikator alami.
|
Kegiatan Pendahuluan
1. Orientasi
2. Apersepsi
3. Motivasi
4. Pemberian Acuan
Kegiatan Inti
1. Stimulation
(stimullasi/ pemberian rangsangan)
2. Problem statemen
(pertanyaan/identifikasi
masalah)
3. Data collection
(pengumpulan data)
4. Data processing
(pengolahan Data)
5. Verification / Pembuktian
6. Generalizatio
(menarik kesimpulan)
Penutup
|
Sumber Belajar :
© Kementerian Pendidikan dan Kebudayaan. 2016. Buku Siswa Mata Pelajaran IPA. Jakarta: Kementerian Pendidikan dan Kebudayaan.
Alat Peraga :
1. Laptop
2. LCD
3. Slide
4. kertas lakmus
5. bahan lainnya yang mendukung
|
Penilaian :
1. Pengetahuan
2. Ketrampilan
|
Materi Ajar
Klasifikasi Materi dan Perubahannya
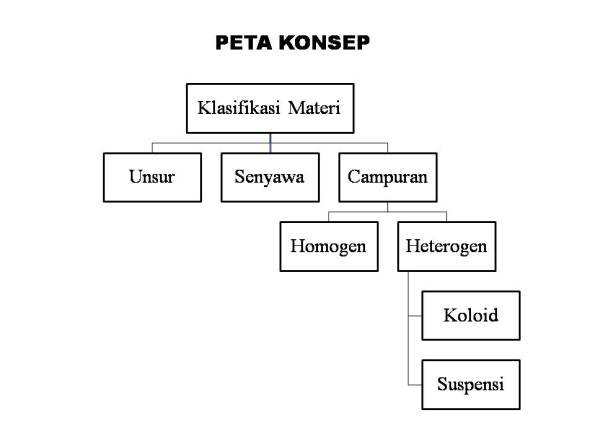 A. UNSUR
A. UNSUR
Konsep: Unsur adalah zat tunggal yang tidak dapat diuraikan lagi menjadi zat lain dengan reaksi kimia biasa.
Materi tersusun dari beberapa partikel penyusun. Para
ilmuwan mengklasifikasikan zat atau materi menjadi dua kelompok, yaitu:
zat tunggal dan campuran. Unsur dan senyawa termasuk dalam golongan zat
tunggal. Nah, apa yang dimaksud dengan unsur? Unsur terdiri dari logam
dan non logam.
Zat murni memiliki sifat yang membedakan dengan zat lainnya.
Misal, unsur hidrogen hanya tersusun dari atom-atom hidrogen saja. Unsur
oksigen hanya tersusun dari atom-atom oksigen saja. Sifat oksigen dan
hidrogen tidak tampak pada zat yang dibentuk dari keduanya, misal air
(H2O). Di alam terdapat 92 jenis unsur alami, sedangkan selebihnya
adalah unsur buatan. Jumlah keseluruhan unsur di alam kira-kira 106
jenis unsur.
Unsur dikelompokkan menjadi tiga (3) bagian, yaitu :
1. Unsur logam
Secara umum unsur logam memiliki sifat berwarna putih
mengkilap, mempunyai titik lebur rendah, dapat menghantarkan arus
listrik, dapat ditempa dan dapat menghantarkan kalor atau panas. Pada
umumnya logam merupakan zat padat, namun terdapat satu unsur logam
yang berwujud cair yaitu air raksa. Beberapa unsur logam yang
bermanfaat dalam kehidupan sehari–hari, antara lain:
a. Khrom (Cr) Digunakan untuk bumper mobil, dan campuran dengan baja menjadi stainless steel.
b. Besi (Fe) Merupakan logam yang paling murah, sebagai campuran
dengan karbon menghasilkan baja untuk konstruksi bangunan, mobil dan rel
kereta api.
c. Nikel ( Ni ) Nikel padat sangat tahan terhadap udara dan air pada
suhu biasa, oleh karena itu nikel digunakan sebagai lapisan pelindung
dengan cara disepuh.
d. Tembaga (Cu) Tembaga banyak digunakan pada kabel listrik, perhiasan,
dan uang logam. Campuran tembaga dengan timah menghasilkan
perunggu sedangkan campuran tembaga dengan seng menghasilkan kuningan.
e. Seng (Zn) Seng dapat digunakan sebagai atap rumah, perkakas rumah tangga, dan pelapis besi untuk mencegah karat.
f. Platina (Pt) Platina digunakan pada knalpot mobil, kontak listrik,
dan dalam bidang kedokteran sebagai pengaman tulang yang patah.
g. Emas (Au) Emas merupakan logam sangat tidak reaktif, dan ditemukan
dalam bentuk murni. Emas digunakan sebagai perhiasan dan
komponen listrik berkualitas tinggi. Campuran emas dengan perak
banyak digunakan sebagai bahan koin.
2. Unsur non logam
Pada umumnya unsur non logam memiliki sifat tidak mengkilap, penghantar
arus listrik yang buruk, dan tidak dapat ditempa. Secara umum non logam
merupakan penghantar panas yang buruk, namun terdapat satu unsur non
logam yang dapat menghantarkan panas dengan baik yaitu grafit. Beberapa
unsur non logam yang bermanfaat dalam kehidupan sehari–hari, antara
lain:
a. Fluor (F) Senyawa fluorid yang dicampur dengan pasta gigi
berfungsi menguatkan gigi, freon – 12 sebagai pendingin kulkas dan AC.
b. Brom (Br) Senyawa brom digunakan sebagai obat penenang saraf, film fotografi, dan bahan campuran zat pemadam kebakaran
c. Yodium (I) Senyawa yodium digunakan sebagai antiseptik luka,
tambahan yodium dalam garam dapur, dan sebagai bahan tes
amilum (karbohidrat) dalam industri tepung
3. Unsur semi logam (Metaloid)Unsur
semi logam memiliki sifat antara logam dan non logam. Beberapa unsur
semi logam yang bermanfaat dalam kehidupan sehari–hari, antara lain :
a. Silikon (Si) Terdapat di alam terbanyak kedua setelah oksigen, yakni
28 %dari kerak bumi. Senyawa silikon banyak digunakan dalam
peralatan pemotong dan pengampelasan, untuk semi konduktor, serta
bahan untuk membuat gelas dan keramik.
b. Germanium ( Ge ) Keberadaan germanium di alam sangat sedikit,
diperoleh dari batu bara dan batuan seng pekat. Germanium merupakan
bahan semikonduktor, yaitu pada suhu rendah berfungsi sebagai
isolator sedangkan pada suhu tinggi sebagai konduktor.
Seorang ahli kimia yang bernama Demitri Mendleev (1834 ~
1907) mengajukan susunan tabel sistem periodik unsur-unsur.
Bagaimanakah nama dan lambang unsur dituliskan? Banyaknya unsur yang
terdapat di alam cukup menyulitkan kita untuk mengingat-ingat nama
unsur. Oleh karena itu, diperlukan suatu tata cara untuk memudahkan kita
mengingat nama unsur tersebut.
Jons Jacob Berzelius (1779 ~ 1848), memperkenalkan tata cara penulisan nama dan lambang unsur, yaitu :
1. Setiap unsur dilambangkan dengan satu huruf yang diambil dari huruf awal nama unsur tersebut.
2. Lambang unsur ditulis dengan huruf kapital.
3. Untuk unsur yang memiliki huruf awal sama, maka penulisan nama dibedakan dengan cara menambah satu huruf di belakangnya dan ditulis dengan huruf kecil.
2. Lambang unsur ditulis dengan huruf kapital.
3. Untuk unsur yang memiliki huruf awal sama, maka penulisan nama dibedakan dengan cara menambah satu huruf di belakangnya dan ditulis dengan huruf kecil.
Contoh: Unsur Karbon ditulis C, oksigen ditulis O, Aluminium ditulis Al, Kalsium ditulis Ca

SENYAWA

Penamaan Senyawa:
Contoh:
NaCl tersusun atas unsur logam Natrium (Na) dan unsur nonlogam Clorin (Cl), sehingga diberi nama Natrium clorida
Jumlah atom disebut dalam bahasa Yunani sebagai berikut:
1 = mono
2 =di
3 = tri
4 = tetra
5 = penta
6 = heksa
7 = hepta
8 = okta
9 = nona
10= deka
Contoh:
N2O diberi nama dinitrogen monoksida
NO diberi nama nitrogen monoksida
N2O5 diberi nama dinitrogen pentaoksida
P2O5 diberi nama diphospor pentaoksida
CCl4 diberi nama carbon tetraklorida
Konsep: Senyawa adalah gabungan dari beberapa unsur yang terbentuk melalui reaksi kimia.
Senyawa memiliki sifat yang berbeda dengan unsur-unsur penyusunnya.
Misal, dua atom hidrogen dengan satu atom oksigen dapat bergabung
membentuk molekul air (H2O). Hidrogen adalah gas yang sangat ringan dan
mudah terbakar, sedangkan oksigen adalah gas yang terdapat di udara yang
sangat diperlukan tubuh kita untuk pembakaran.
Tampak jelas bahwa sifat air berbeda dengan sifat hidrogen dan
oksigen. Contoh lain senyawa adalah garam dapur (NaCl). Garam dapur
disusun oleh unsur natrium dan unsur klor. Natrium memiliki sifat logam
yang ringan, sedangkan klor adalah suatu gas beracun. Dua unsur
tersebut digabung membentuk garam dapur berupa mineral yang
sangat dibutuhkan oleh tubuh kita.
Senyawa termasuk zat tunggal yang tersusun dari beberapa unsur dengan
perbandingan massa tetap. Di alam ini terdapat kurang lebih 10 juta
senyawa. Air (H2O) merupakan senyawa paling banyak terdapat di alam.
Bagaimanakah tata cara penulisan senyawa? Senyawa dituliskan dalam wujud
rumus kimia. Rumus kimia adalah zat yang terdiri dari
kumpulan lambang-lambang unsur dengan komposisi tertentu. Komposisi
tersebut berupa bilangan yang menyatakan jumlah atom penyusunnya
(angka indeks). Misal, suatu senyawa terdiri dari atom unsur natrium
(Na) dan atom unsur klor (Cl). Jika angka indeks masing-masing atom
unsur adalah 1 dan 1, maka rumus kimia senyawa yang dibentuk sebagai
berikut :
Angka indeks Na = 1, angka indeks Cl = 1, Jadi rumus kimia senyawa tersebut adalah NaCl ( Natrium klorida ).
Angka indeks Na = 1, angka indeks Cl = 1, Jadi rumus kimia senyawa tersebut adalah NaCl ( Natrium klorida ).
Rumus kimia dapat berupa rumus molekul dan rumus empiris. Rumus molekul adalah rumus kimia yang menyatakan jenis dan jumlah atom yang menyusun zat. Misal, C2H4 (Etena), H2O (air). Rumus empiris adalah rumus
kimia yang menyatakan perbandingan terkecil jumlah atom–atom pembentuk
senyawa. Misal, rumus kimia C2H4, maka rumus empiris senyawa tersebut
adalah CH2.
Joseph Lonis Proust (1754~1826) seorang ilmuwan dari
Perancis mengemukakan hukum perbandingan tetap atau sering dikenal
dengan hukum Proust, yaitu : perbandingan berat unsur-unsur penyusun
senyawa adalah tetap. Eksperimen yang dilakukan Proust adalah reaksi
antara unsur hidrogen dan oksigen sehingga terbentuk air (H2O). Dari
percobaan yang dilakukan oleh Proust ditarik kesimpulan bahwa:
1. Air tersusun dari oksigen dan hidrogen dengan perbandingan massa unsur oksigen banding hidrogen adalah 8 : 1
2. Jumlah zat sebelum dan sesudah reaksi adalah tetap.
2. Jumlah zat sebelum dan sesudah reaksi adalah tetap.
Senyawa-senyawa baru ditemukan dan dipisahkan dari tumbuh– tumbuhan.
Misal, jeruk diketahui mengandung vitamin C, setelah dilakukan pemisahan
ternyata jeruk mengandung asam askorbat. Struktur vitamin C ditemukan,
maka dilakukan sintesis untuk membuat vitamin C di laboratorium. Rumus
senyawa merupakan gabungan lambang unsur yang menunjukkan jenis unsur
pembentuk senyawa dan jumlah atom masing-masing unsur. Misal, sukrosa
memiliki rumus senyawa C12H22O11. Sukrosa tersusun dari 12 atom karbon,
22 atom hidrogen, dan 11 atom oksigen.

Penamaan Senyawa:
- Senyawa yang Terbentuk dari Unsur Logam dan Nonlogam
Contoh:
NaCl tersusun atas unsur logam Natrium (Na) dan unsur nonlogam Clorin (Cl), sehingga diberi nama Natrium clorida
- Senyawa yang Terbentuk dari Unsur Nonlogam-Nonlogam
Jumlah atom disebut dalam bahasa Yunani sebagai berikut:
1 = mono
2 =di
3 = tri
4 = tetra
5 = penta
6 = heksa
7 = hepta
8 = okta
9 = nona
10= deka
Contoh:
N2O diberi nama dinitrogen monoksida
NO diberi nama nitrogen monoksida
N2O5 diberi nama dinitrogen pentaoksida
P2O5 diberi nama diphospor pentaoksida
CCl4 diberi nama carbon tetraklorida


Komentar
Posting Komentar